Hel (He, łac. Helium) - jest to pierwiastek chemiczny o liczbie atomowej 2, z grupy helowców (gazów szlachetnych) w układzie okresowym. Jest po wodorze drugim najbardziej rozpowszechnionym pierwiastkiem chemicznym we wszechświecie, jednak na Ziemi występuje wyłącznie w śladowych ilościach (4×10−7% w górnych warstwach atmosfery).
 Hel na Ziemi występuje głównie w atmosferze (5,2×10−4% obj. w powietrzu), pochodzi głównie z rozpadu jąder promieniotwórczych w naturalnych szeregach promieniotwórczych. W litosferze hel występuje również w niektórych złożach gazu ziemnego. W gazach występujących w Stanach Zjednoczonych dochodzi do 1%, w gazach występujących w Europieilość ta jest bardzo mała (z wyjątkiem Polski – do 3%). Praktycznie cały hel, który mógł pierwotnie istnieć na Ziemi, nie mogąc związać się z żadnym innym pierwiastkiem, jako bardzo lekki opuścił atmosferę Ziemi.
Hel na Ziemi występuje głównie w atmosferze (5,2×10−4% obj. w powietrzu), pochodzi głównie z rozpadu jąder promieniotwórczych w naturalnych szeregach promieniotwórczych. W litosferze hel występuje również w niektórych złożach gazu ziemnego. W gazach występujących w Stanach Zjednoczonych dochodzi do 1%, w gazach występujących w Europieilość ta jest bardzo mała (z wyjątkiem Polski – do 3%). Praktycznie cały hel, który mógł pierwotnie istnieć na Ziemi, nie mogąc związać się z żadnym innym pierwiastkiem, jako bardzo lekki opuścił atmosferę Ziemi.
Występuje w postaci dwóch izotopówtrwałych – 3He i 4He. Znanych jest także kilka syntetycznych izotopów nietrwałych (T½ < 1 sekundy), z których najbardziej stabilne są 6He i 8He.
Hel jest najmniej aktywnym pierwiastkiem chemicznym, z najwyższą spośród wszystkich pierwiastków energią jonizacji (24,59 eV). Znane są jego związki metastabilne (np. HHeF, (HeO)(CsF) i LiHe) i krótko żyjące cząsteczki HeNe i jony He+ oraz He2+ .Tworzy też stabilne stałe związki międzycząsteczkowe, np. NeHe2 i He@H2O. Na przełomie 2016/2017 doniesiono o otrzymaniu pierwszego stałego związku helu, Na2He, który jest trwały termodynamicznie pod ciśnieniem powyżej 113 GPa (ok. 1,1×106 atm). Tworzy kryształy o strukturze fluorytu.
Nie ma żadnego znaczenia biologicznego.
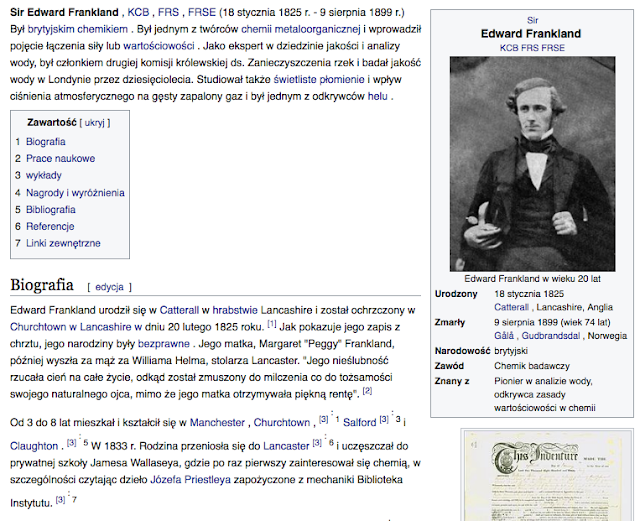
Odkrycie helu: Hel odkryto najpierw na Słońcu, później na Ziemi. Podczas całkowitego zaćmienia Słońca, które miało miejsce 18 sierpnia 1868 roku i było widoczne w Indiach, astronom Pierre Janssen, badając widmo korony słonecznej, zaobserwował pomarańczowy prążek odpowiadający długości fali 587,6 nm, którego nie można było przypisać do żadnego spośród znanych wówczas pierwiastków. Ten sam prążek w widmie Słońca zaobserwował 20 października1868 r. angielski astronom Norman Lockyer. Lockyer i angielski chemik Edward Frankland nadali nowemu pierwiastkowi – emitującemu falę o długości 587,6 nm – nazwę helium od greckiego boga słońca – Heliosa. Przez wiele lat hel był uważany za pierwiastek, który występuje na Słońcu, ale nie występuje na Ziemi. W roku 1895 William Ramsay otrzymał hel po potraktowaniu kleweitu (rudy uranowej) kwasem mineralnym. Ramsay przesłał próbkę gazu do Williama Crookesa i Normana Lockyera, którzy zidentyfikowali hel.
Hel stały: Hel jako jedyny pierwiastek pozostaje ciekły nawet w temperaturze zera bezwzględnego (pod ciśnieniem atmosferycznym) i zestala się dopiero w podwyższonym ciśnieniu. Ma najniższą temperaturę krzepnięcia spośród wszystkich pierwiastków: <0,95 K (pod ciśnieniem 26 atm). W zależności od ciśnienia hel w stanie stałym może zmieniać objętość o 30%. W temperaturze poniżej 0,2-0,4 K hel stały przechodzi przemianę fazową do formy o właściwościach nadciekłych ("hel nadstały").
Zastosowania helu:
- Hel w postaci ciekłej jest używany do chłodzenia tam, gdzie potrzebne są ekstremalnie niskie temperatury, ze względu na jego bardzo niską temperaturę wrzenia. Stosuje się go m.in. do chłodzenia nadprzewodników.
- Jako najlżejszy gaz bezpieczny (niepalny) był stosowany do wypełniania statków powietrznych lżejszych od powietrza, czyli aerostatów (balony, sterowce). Obecnie ze względu na wysokie koszty jego pozyskania, zamiast helu stosuje się w aerostatach najczęściej ogrzane powietrze.
- Ze względu na niską rozpuszczalność w osoczu krwi, używany jest jako składnik mieszanki do oddychania w głębokim nurkowaniu.
- Hel jest używany jako gaz napędowy w balonach do kontrapulsacji wewnątrzaortalnej (cewnik zakończony balonem wprowadzany jest do aorty najczęściej przez tętnicę udową, napełnianie i opróżnianie balonu gazem zgodnie z rytmem serca wspomaga niewydolne krążenie).
- Hel w mieszaninie z tlenem może być używany do wentylacji mechanicznej pacjentów z ciężką obturacją oskrzeli. Hel ma znacznie mniejszą gęstość niż azot. Zastąpienie azotu helem obniża liczbę Reynoldsa i zmienia charakter przepływu gazów w drogach oddechowych z turbulentnego na laminarny co istotnie obniża opory przepływu. Metoda ma charakter eksperymentalny i nie została wdrożona do powszechnej praktyki klinicznej.
Liczba Reynoldsa (ang. Reynolds number) – jedna z liczb podobieństwa stosowanych w mechanice płynów (hydrodynamice, aerodynamice i reologii). Liczba ta pozwala oszacować występujący podczas ruchu płynu stosunek sił bezwładności do sił lepkości. Liczba Reynoldsa stosowana jest jako podstawowe kryterium stateczności ruchu płynów.
- Hel dostarczony do płuc powoduje zmianę wysokości głosu - dzieje się tak, ponieważ częstość drgań strun głosowych w komorze rezonansowej, jaką jest krtań, ściśle zależy od gęstości ośrodka, w którym te drgania zachodzą (prędkość dźwięku w helu jest ok. 3 razy większa niż w powietrzu). Przeciwny efekt ma wdychanie ksenonu.
- Hipotetycznie izotop 3He może zostać wykorzystany w kontrolowanej reakcji termojądrowej z deuterem do uzyskiwania energii bez powstawania niepożądanych odpadów promieniotwórczych. Na Ziemi 3He występuje jedynie śladowo, natomiast znaczne ilości tego izotopu występować mogą w gruncie księżycowym, w związku z czym rozważane są projekty jego wydobycia i transportu z Księżyca na Ziemię.
Związki helu:




































Brak komentarzy:
Prześlij komentarz