HYDROKSYKWASY, CD.:
Spalanie glukozy z dostatecznym udziałem tlenu:
- C
6H
12O
6 + 6O
2 → 6CO
2 + 6H
2O z jednej cząsteczki glukozy powstają 33 cząsteczki ATP - Spalanie glukozy przy niedoborze tlenu:
- C
6H
12O
6 → 2C
2H
4OHCOOH z jednej cząsteczki glukozy powstają 2 cząsteczki ATP - Wzrastające stężenie kwasu mlekowego odbiera się jako doznanie bólu w trakcie intensywnego wysiłku. Kwas ten jednak dość szybko odprowadzany jest z mięśni przez układ krwionośny, a następnie ponownie przetwarzany głównie w wątrobie do glukozy w procesie zwanym glukoneogenezą lub cyklem Corich. W zasadzie po 2 godzinach od ustania intensywnego wysiłku fizycznego cały kwas mlekowy jest odprowadzany z mięśni. Glukoneogeneza wymaga dostarczenia energii pochodzącej z oddychania tlenowego. Dzięki wytwarzaniu kwasu mlekowego mięsień może chwilowo osiągnąć moc przekraczającą maksymalną wydajność układów krążenia i oddechowego. Niestety gromadzenie się kwasu mlekowego szybko zmusza do przetrwania wysiłku. Jeśli wysiłek nie przekracza możliwości dostarczania tlenu przez układ krążenia kwas mlekowy nie powstaje. Zjwisko może dotyczyć całego organizmu, jak i pojedynczego mięśnia. Kwas mlekowy jest atraktantem dla komarów, co sprawia, że osoby w trakcie lub po wysiłku fizycznym są bardziej narażone na ich ukąszenia. Kwas mlekowy ma znaczenie w patomechanizmie wielu chorób. Wszelkie zaburzenia oddychania tlenowego prowadzą do gromadzenia się kwasu mlekowego i kwasicy.
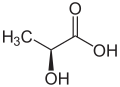
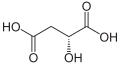 14) Kwas jabłkowy (kwas hydroksybursztynowy, łac. Acidum malicum) - jest to organiczny związek chemiczny, hydroksywkas dikarboksylowy występujący m.in. w jabłkach i rabarbarze. Jest on produktem ubocznym metabolizmu węglowodanów. Jego forma zjonizowana (jabłczan) występuje jako produkt pośredni w cyklu kwasu cytrynowego (cyklu Krebsa). Zawiera jedno centrum stereogeniczne i jego cząsteczka jest chiralna. Naturalnie występuje enacjomer o konfiguracji L. Syntetyczny kwas jabłkowy jest racematem (mieszanina racemiczna to równomolowa mieszanina pary enacjomerów danego związku chemicznego).
14) Kwas jabłkowy (kwas hydroksybursztynowy, łac. Acidum malicum) - jest to organiczny związek chemiczny, hydroksywkas dikarboksylowy występujący m.in. w jabłkach i rabarbarze. Jest on produktem ubocznym metabolizmu węglowodanów. Jego forma zjonizowana (jabłczan) występuje jako produkt pośredni w cyklu kwasu cytrynowego (cyklu Krebsa). Zawiera jedno centrum stereogeniczne i jego cząsteczka jest chiralna. Naturalnie występuje enacjomer o konfiguracji L. Syntetyczny kwas jabłkowy jest racematem (mieszanina racemiczna to równomolowa mieszanina pary enacjomerów danego związku chemicznego). - Podczas ogrzewania bez dostępu powietrza ulega dehydratacji do mieszaniny kwasu fumarowego i kwasu maleinowego. Stosuje się go w przemyśle spożywczym jako konserwant oraz w przemyśle farmaceutycznym.
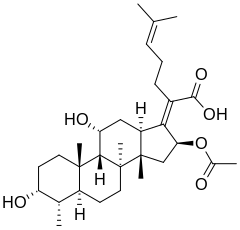 15) Kwas fusydynowy (łac. Acidum fusidicum) - jest to organiczny związek chemiczny, naturalny antybiotyk bakteriostatyczny o budowie steroidowej. Mechanizm jego działania polega na hamowaniu syntezy białka bakterii. Podczas stosowania kwasu fusydynowego szybko dochodzi do powstawania oporności bakterii na ten antybiotyk, dlatego zaleca się stosowanie go w połączeniach z innymi antybiotykami, najlepiej z takimi, z którymi wykazuje działanie synergistyczne (cefalosporyny, penicyliny izoksazolinowe, wankomycyna ryfampicyna). Nie należy natomiast łączyć kwasu fusydynowego z fluorochinolonami, ponieważ wykazują one między sobą działanie antagonistyczne. Kwas fusydynowy wykazuje również oporność krzyżową z cefalosporynami Po raz pierwszy kwas fusydynowy udało się uzyskać w 1960 roku w duńskim mieście Ballerup z hodowli grzyba Fussidium coccineum izolowanego z kału małpy. Po raz pierwszy został wprowadzony do terapii w 1862 roku w Danii. Kwas fusydynowy jest stosowany głównie na Staphyloococcus aureus (działa on na szczepy MRSA). Oprócz tych bakterii jest on skuteczny również na Neisseria meningitidis, Niesseria gonorrhoeae, Bordetella petussis, Corynebacterium diphteriae, Clostridium difficile, Mycobacterium leprae (również słaba aktywność w stosunku do Mycobacterium tuberculosis).
15) Kwas fusydynowy (łac. Acidum fusidicum) - jest to organiczny związek chemiczny, naturalny antybiotyk bakteriostatyczny o budowie steroidowej. Mechanizm jego działania polega na hamowaniu syntezy białka bakterii. Podczas stosowania kwasu fusydynowego szybko dochodzi do powstawania oporności bakterii na ten antybiotyk, dlatego zaleca się stosowanie go w połączeniach z innymi antybiotykami, najlepiej z takimi, z którymi wykazuje działanie synergistyczne (cefalosporyny, penicyliny izoksazolinowe, wankomycyna ryfampicyna). Nie należy natomiast łączyć kwasu fusydynowego z fluorochinolonami, ponieważ wykazują one między sobą działanie antagonistyczne. Kwas fusydynowy wykazuje również oporność krzyżową z cefalosporynami Po raz pierwszy kwas fusydynowy udało się uzyskać w 1960 roku w duńskim mieście Ballerup z hodowli grzyba Fussidium coccineum izolowanego z kału małpy. Po raz pierwszy został wprowadzony do terapii w 1862 roku w Danii. Kwas fusydynowy jest stosowany głównie na Staphyloococcus aureus (działa on na szczepy MRSA). Oprócz tych bakterii jest on skuteczny również na Neisseria meningitidis, Niesseria gonorrhoeae, Bordetella petussis, Corynebacterium diphteriae, Clostridium difficile, Mycobacterium leprae (również słaba aktywność w stosunku do Mycobacterium tuberculosis). - 16) Kwas migdałowy - aromatyczny hydroksykwas karboksylowy.
-
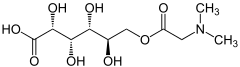 17) Kwas pangamowy (witamina B15) - jest to związek chemiczny zaliczany dawniej do grupy witamin, pochodna kwasu glukonowego. Bierze on udział w procesach transmetylacji w reakcjach oddychania komórkowego oraz zwiększa wydzielanie kortykosterydów. Dawniej uważano, że w strukturze kwasu pangamowego atom azotu podstawiony jest dwiema grupami izopropylowymi, a nie metylowymi. Nie ma dowodów na to, że kwas pangamowy spełnia definicję witaminy, czyli niezbędnego składnika odżywczego, a nawet że nie jest szkodliwy.
17) Kwas pangamowy (witamina B15) - jest to związek chemiczny zaliczany dawniej do grupy witamin, pochodna kwasu glukonowego. Bierze on udział w procesach transmetylacji w reakcjach oddychania komórkowego oraz zwiększa wydzielanie kortykosterydów. Dawniej uważano, że w strukturze kwasu pangamowego atom azotu podstawiony jest dwiema grupami izopropylowymi, a nie metylowymi. Nie ma dowodów na to, że kwas pangamowy spełnia definicję witaminy, czyli niezbędnego składnika odżywczego, a nawet że nie jest szkodliwy.  18) Kwas pantotenowy - jest to organiczny związek chemiczny, bardzo rozpowszechniony w świecie roślinnym i zwierzęcym (cząstka pan oznacza "wszystko", "wszech-", a pantotenowy to inaczej "wszechobecny"). Jest on niezbędna dla każdej żywej komórki, ale w stanie wolnym rzadko występuje w przyrodzie. Chemicznie kwas pantotenowy jest amidem kwasu pantoinowego i beta-alaniny. Kwas pantotenowy czasami jest błędnie utożsamiany z witaminą B5. W rzeczywistości witamina B5 to mieszanina następujących związków chemicznych: kwasu pantotenowego, panteiny (pochodnej kwasu pantotenowego), pantenolu (należącego do grupy alkoholi, nie występującego w przyrodzie, ale aktywnego biologicznie w stosunku do ludzi i zwierząt), koenzymu A (aktywnej biologicznie formy kwasu pantotenowego). Po wchłonięciu kwas pantotenowy ulega następującym przemianom: a) fosforylacja - odpowiednie kinazy tworzą kwas fosfopantotenowy; b) przyłączenie cysteiny, powstaje pantotenylocysteina; c) dekarb
18) Kwas pantotenowy - jest to organiczny związek chemiczny, bardzo rozpowszechniony w świecie roślinnym i zwierzęcym (cząstka pan oznacza "wszystko", "wszech-", a pantotenowy to inaczej "wszechobecny"). Jest on niezbędna dla każdej żywej komórki, ale w stanie wolnym rzadko występuje w przyrodzie. Chemicznie kwas pantotenowy jest amidem kwasu pantoinowego i beta-alaniny. Kwas pantotenowy czasami jest błędnie utożsamiany z witaminą B5. W rzeczywistości witamina B5 to mieszanina następujących związków chemicznych: kwasu pantotenowego, panteiny (pochodnej kwasu pantotenowego), pantenolu (należącego do grupy alkoholi, nie występującego w przyrodzie, ale aktywnego biologicznie w stosunku do ludzi i zwierząt), koenzymu A (aktywnej biologicznie formy kwasu pantotenowego). Po wchłonięciu kwas pantotenowy ulega następującym przemianom: a) fosforylacja - odpowiednie kinazy tworzą kwas fosfopantotenowy; b) przyłączenie cysteiny, powstaje pantotenylocysteina; c) dekarb- oksylacja przyłączonej cysteiny - powstaje fosfopantoteina.
- Kwas pantotenowy jest niezbędny do prawidłowego metabolizmu białek, cukrów i tłuszczów oraz do syntezy niektórych hormonów, przyspiesza gojenie ran, warunkuje prawidłowy przebieg procesu uwalniania energii, zapobiega przemęczeniu i usprawnia układ sercowo-naczyniowy, nerwowy i pokarmowy, bierze udział w wytwarzaniu tłuszczów, cholesterolu, hormonów i przekaźników nerwowych, uczestniczy w regeneracji tkanek, poprawia pigmentację i stan włosów. Skutkami niedoboru kwasu pantotenowego są zaburzenia układu nerwowego, trudności z nauką, nadmierna drażliwość, omdlenia, depresje, utrata koordynacji, bóle i sztywność w ramionach i nogach, niepewny chód, wypadanie włosów, przedwczesna siwizna, łysienie, zmiany skórne, uczucie pieczenia, kłopoty ze wzrokiem, pęknięcia skóry w kącikach ust i oczu, zaburzenia układu trawiennego, utrata apetytu, obstrukcja, niestrawność, przemęczenie, podatność na zakażenia, złe gojenie się ran, częste infekcje górnych dróg oddechowych, zaburzenia układu sercowo-naczyniowego, przyspieszenie czynności serca. Nadmiar nie jest toksyczny, lecz może powodować biegunki Źródłami kwasu pantotenowego są wątróbka, otręby pszenne, ryby (np. śledzenie, makrele, pstrągi), grzyby, mleko pełne, mięso kurczaka, mleczko pszczele, pestki słonecznika, sery, orzechy, jajka, owoce awokado, pomarańcze, ziemniaki, brokuły, ciemny ryż, melony, pełnoziarnisty chleb, soja, masło orzechowe, banany, yerba mate.
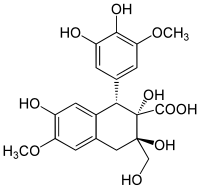 19) Kwas plikatowy - jest to organiczny związek chemiczny z grupy hydroksykwasów. Jest kwasem żywicznym z olejku cedrowego. Występuje również w żywotniku olbrzymim. Olejek cedrowy to tani olejek eteryczny (ciekła, lotna substancja zapachowa znajdująca się najczęściej w specjalnych komórkach tkanki wydzielniczej roślin. Takie komórki są charakterystyczne dla roślin olejkodajnych, na przykład gatunków z rodziny sosnowatych, jasnotowatych, mirtowatych, rutowatych i baldaszkowatych. Pod względem składu olejek jest mieszaniną rozmaitych związków chemicznych, jak ketony, aldehydy, alkohole, estry, laktony, terpeny, oraz innych związków organicznych, w tym zawierających azot i siarkę związków o nieprzyjemnym zapachy (aminy, tiole); do połowy XX wieku olejki były uważane przez botaników za produkt odpadowy przemiany materii, niemający wpływu na rozwój roślin. Sytuacja uległa zmianie z chwilą opublikowania pracy Fraenkla (1959 r.), który stwierdził, że metabolity wtórne decydują ożywieniowych zachowaniach owadów. Spostrzeżenie zapoczątkowało intensywny rozwój badań w dziedzinie ekologii, dotyczących koewolucji biochemicznej zwierząt i roślin oraz roli substancji semiochemicznych w kształtowaniu struktury współczesnych ekosystemów), pozuyskiwany z drewna jałowca wirgińskiego (cdru wirgińskiego) metodą destylacji z parą wodną. Niektóre rodzaje olejków, nazywanych cedrowymi, otrzymuje się również z innych surowców, np. z drewna cedru atlaskiego (łac. Cedrus atlantica) lub z liści żywotnika zachodniego (łac. Thuja occidentalis L., biały cedr). Głównymi składnikami olejku są cedren, dedrol (kamfora cedrowa), pseudocedrol, cedroneol i seskwiterpeny. Olejek cedrowy jest stosowany jako środek zapachowy oraz jako ciecz immersyjna w mikroskopii. Olejek ten nie jest fałszowany ze względu na swą niską cenę. Stosowany jest jako ciecz immersyjna (immersja, z łac. immergo - zanurzam - to metoda stosowana w mikroskopii w celu zwiększenia zdolności rozdzielczej mikroskopu optycznego - polega ona na wypełnieniu przestrzeni pomiędzy preparatem a obiektywem mikroskopu przeźroczystym płynem (cieczą imersyjną) o współczyniku załamania zbliżonym do współczynnika załamania szkła soczewki - jest to często olejek cedrowy. Zapobiega to załamywaniu się światła po przejściu ze środowiska optycznie gęstszego - szkła do środowiska optycznie rzadszego - powietrza i zaciemnieniu pola widzenia - zwiększana jest apertura liczbowa obiektywu mikroskopu), dzięki swej bardzo dużej wartości współczynnika załamania światła. Wypełnienie przestrzeni między preparatem a obiektywem taką przezroczystą cieczą zapobiega niekorzystnemu załamywaniu się światła na granicy między szkłem i powietrzem. Olejek jest też stosowany do perfumowania mydeł toaletowych i jako utrwalacz kompozycji zapachowych (np. kwiatowych, tj. jaśmin, mimoza).
19) Kwas plikatowy - jest to organiczny związek chemiczny z grupy hydroksykwasów. Jest kwasem żywicznym z olejku cedrowego. Występuje również w żywotniku olbrzymim. Olejek cedrowy to tani olejek eteryczny (ciekła, lotna substancja zapachowa znajdująca się najczęściej w specjalnych komórkach tkanki wydzielniczej roślin. Takie komórki są charakterystyczne dla roślin olejkodajnych, na przykład gatunków z rodziny sosnowatych, jasnotowatych, mirtowatych, rutowatych i baldaszkowatych. Pod względem składu olejek jest mieszaniną rozmaitych związków chemicznych, jak ketony, aldehydy, alkohole, estry, laktony, terpeny, oraz innych związków organicznych, w tym zawierających azot i siarkę związków o nieprzyjemnym zapachy (aminy, tiole); do połowy XX wieku olejki były uważane przez botaników za produkt odpadowy przemiany materii, niemający wpływu na rozwój roślin. Sytuacja uległa zmianie z chwilą opublikowania pracy Fraenkla (1959 r.), który stwierdził, że metabolity wtórne decydują ożywieniowych zachowaniach owadów. Spostrzeżenie zapoczątkowało intensywny rozwój badań w dziedzinie ekologii, dotyczących koewolucji biochemicznej zwierząt i roślin oraz roli substancji semiochemicznych w kształtowaniu struktury współczesnych ekosystemów), pozuyskiwany z drewna jałowca wirgińskiego (cdru wirgińskiego) metodą destylacji z parą wodną. Niektóre rodzaje olejków, nazywanych cedrowymi, otrzymuje się również z innych surowców, np. z drewna cedru atlaskiego (łac. Cedrus atlantica) lub z liści żywotnika zachodniego (łac. Thuja occidentalis L., biały cedr). Głównymi składnikami olejku są cedren, dedrol (kamfora cedrowa), pseudocedrol, cedroneol i seskwiterpeny. Olejek cedrowy jest stosowany jako środek zapachowy oraz jako ciecz immersyjna w mikroskopii. Olejek ten nie jest fałszowany ze względu na swą niską cenę. Stosowany jest jako ciecz immersyjna (immersja, z łac. immergo - zanurzam - to metoda stosowana w mikroskopii w celu zwiększenia zdolności rozdzielczej mikroskopu optycznego - polega ona na wypełnieniu przestrzeni pomiędzy preparatem a obiektywem mikroskopu przeźroczystym płynem (cieczą imersyjną) o współczyniku załamania zbliżonym do współczynnika załamania szkła soczewki - jest to często olejek cedrowy. Zapobiega to załamywaniu się światła po przejściu ze środowiska optycznie gęstszego - szkła do środowiska optycznie rzadszego - powietrza i zaciemnieniu pola widzenia - zwiększana jest apertura liczbowa obiektywu mikroskopu), dzięki swej bardzo dużej wartości współczynnika załamania światła. Wypełnienie przestrzeni między preparatem a obiektywem taką przezroczystą cieczą zapobiega niekorzystnemu załamywaniu się światła na granicy między szkłem i powietrzem. Olejek jest też stosowany do perfumowania mydeł toaletowych i jako utrwalacz kompozycji zapachowych (np. kwiatowych, tj. jaśmin, mimoza).  20) Kwas rycynolowy - jest to organiczny związek chemiczny, nienasycony hydroksykwas karboksylowy. Otrzymywany jest on z oleju rycynowego (łac. Oleum Ricini) jako główny jego składnik (80%) i stosowany w syntezie chemicznej. Estry kwasu rycynolowego wykorzystywane są jako środki powierzchniowo czynne w przemyśle tekstylnym. Kwas rycynolowy oraz tworzące się stopniowo w środowisku jelit jego sole sodowe i potasowe (mydła rycynolowe) są głównie odpowiedzialne za przeczyszczające działanie oleju rycynowego. Występuje on w elajosomach różnych gatunków roślin,w których pełni funkcję wabiącą mrówki.
20) Kwas rycynolowy - jest to organiczny związek chemiczny, nienasycony hydroksykwas karboksylowy. Otrzymywany jest on z oleju rycynowego (łac. Oleum Ricini) jako główny jego składnik (80%) i stosowany w syntezie chemicznej. Estry kwasu rycynolowego wykorzystywane są jako środki powierzchniowo czynne w przemyśle tekstylnym. Kwas rycynolowy oraz tworzące się stopniowo w środowisku jelit jego sole sodowe i potasowe (mydła rycynolowe) są głównie odpowiedzialne za przeczyszczające działanie oleju rycynowego. Występuje on w elajosomach różnych gatunków roślin,w których pełni funkcję wabiącą mrówki. - KETOKWASY:
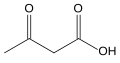 1) Kwas acetylooctowy (CH3-CO-CH2-COOH-) - jest to organiczny związek chemiczny, najprostszy beta-ketokwas. Występuje on w organizmie człowieka jako produkt pośredni metabolizmu tłuszczów. Łatwo ulega on rozkładowi do dwutlenku węgla i acetonu. Stosowany jest w syntezie do otrzymywania związków organicznych.
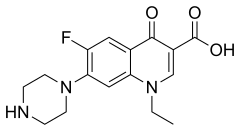
1) Kwas acetylooctowy (CH3-CO-CH2-COOH-) - jest to organiczny związek chemiczny, najprostszy beta-ketokwas. Występuje on w organizmie człowieka jako produkt pośredni metabolizmu tłuszczów. Łatwo ulega on rozkładowi do dwutlenku węgla i acetonu. Stosowany jest w syntezie do otrzymywania związków organicznych. 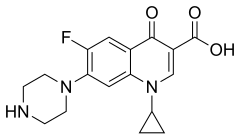 2) Cyprofloksacyna - jest to chemioterapeutyk z grupy chinolonów II generacji (fluorochinlonów), o działaniu bakteriobójczym, wykazujący swoje działanie poprzez zaburzanie replikacji DNA bakterii w wyniku zahamowania syntezy DNA. Jest najsilniej działającym lekiem wśród fluorochinolonów. Cyprofloksacyna jest wydalana głównie w postaci niezmienionej z moczem i częściowo z kałem, osiągając w nich duże stężenia.
2) Cyprofloksacyna - jest to chemioterapeutyk z grupy chinolonów II generacji (fluorochinlonów), o działaniu bakteriobójczym, wykazujący swoje działanie poprzez zaburzanie replikacji DNA bakterii w wyniku zahamowania syntezy DNA. Jest najsilniej działającym lekiem wśród fluorochinolonów. Cyprofloksacyna jest wydalana głównie w postaci niezmienionej z moczem i częściowo z kałem, osiągając w nich duże stężenia.- Zakres działania bakteriobójczego Cyprofloksacyny:
- - SZCZEGÓLNIE SILNIE BIOBÓJCZA WOBEC BAKTERII GRAM-UJEMNYCH,
- - PRĄTKI GRUŹLICY, PRĄTKI TYPOWE,
- - SALMONELLA, SHIGELLA,
- - PSEUDOMONAS AERUGINOSA,
- - ESCHERICHIA COLI
- Wskazana jest w przypadku leczenia zakażeń drobnoustrojami wrażliwymi na cyprofloksacynę. Stosowana jest głównie w leczeniu zakażeń układu moczowego. Z uwagi na to, że dobrze przenika do płuc, gruczołu krokowego, kości, płynu mózgowo-rdzeniowego, migdałków podniebiennych, jest stosowana w zakażeniach tych narządów. Jest skuteczna również w leczeniu duru brzusznego i zakażeń wąglikiem.
 3) Enrofloksacyna - jest to antybiotyk z grupy fluorochinolonów, który jako pierwszy został dopuszczony do stosowania w leczeniu zwierząt domowych. Działanie enrofloksacyny polega na inhibicji bakteryjnej gyrazy DNA, enzymu warunkującego tworzenie spirali DNA. Wysoką biodostępność uzyskuje się zarówno poprzez doustne, jak również pozajelitowe podania leku Wydalanie substancji z organizmu zachodzi głównie przez nerki. Biologiczny okres półtrwania zależy od gatunku zwierzęcia i waha się od 2 do 7 godzin. Głównym metabolitem jest cyprofloksacyna. U psów stopień przemiany metabolicznej kształtuje się na poziomie ponad 40%. Enrofloksacyna jest stosowana jako chemioterapeutyk w chorobach zakaźnych u psów, kur domowych, kotów, cieląt, krów, świń, indyków, małych zwierząt domowych. Wykazuje wysoką skuteczność przeciwko dużej liczbie zarówno G-dodatnich, jak również G-ujemnych patogenów, takich jak: Escherichia coli, Erysipelothrix rhusipathie, Haemophilus spp., Salmonella spp., Pasteurella spp. i Staphylococcus, oraz mykoplazm (Mycoplasma bovis i Mycoplasma hyopneumoniae) w zależności od gatunku zwierzęcia, stosuje się ją do leczenia różnych chorób
3) Enrofloksacyna - jest to antybiotyk z grupy fluorochinolonów, który jako pierwszy został dopuszczony do stosowania w leczeniu zwierząt domowych. Działanie enrofloksacyny polega na inhibicji bakteryjnej gyrazy DNA, enzymu warunkującego tworzenie spirali DNA. Wysoką biodostępność uzyskuje się zarówno poprzez doustne, jak również pozajelitowe podania leku Wydalanie substancji z organizmu zachodzi głównie przez nerki. Biologiczny okres półtrwania zależy od gatunku zwierzęcia i waha się od 2 do 7 godzin. Głównym metabolitem jest cyprofloksacyna. U psów stopień przemiany metabolicznej kształtuje się na poziomie ponad 40%. Enrofloksacyna jest stosowana jako chemioterapeutyk w chorobach zakaźnych u psów, kur domowych, kotów, cieląt, krów, świń, indyków, małych zwierząt domowych. Wykazuje wysoką skuteczność przeciwko dużej liczbie zarówno G-dodatnich, jak również G-ujemnych patogenów, takich jak: Escherichia coli, Erysipelothrix rhusipathie, Haemophilus spp., Salmonella spp., Pasteurella spp. i Staphylococcus, oraz mykoplazm (Mycoplasma bovis i Mycoplasma hyopneumoniae) w zależności od gatunku zwierzęcia, stosuje się ją do leczenia różnych chorób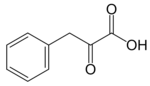 4) Kwas fenylopirogronowy (fenyloketon) - jest to organiczny związek chemiczny z grupy alfa-ketokwasów karboksylowych, fenylowa pochodna kwasu pirogronowego. Jest metabolitem fenyloalaniny i występuje w podwyższonym stężeniu u chorych na fenyloketonurię. Można go otrzymać z chlorku benzylu, tlenku węgla i wody w reakcji katalizowanej oktakarbonylkiem dikobaltu wobec wodorotlenku wapnia.
4) Kwas fenylopirogronowy (fenyloketon) - jest to organiczny związek chemiczny z grupy alfa-ketokwasów karboksylowych, fenylowa pochodna kwasu pirogronowego. Jest metabolitem fenyloalaniny i występuje w podwyższonym stężeniu u chorych na fenyloketonurię. Można go otrzymać z chlorku benzylu, tlenku węgla i wody w reakcji katalizowanej oktakarbonylkiem dikobaltu wobec wodorotlenku wapnia.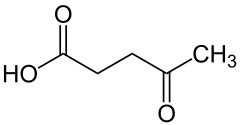 5) Kwas lewulinowy (kwas 4-oksowalerianowy lub kwas gamma-oksowalerianowy) - jest to organiczny związek chemiczny, najprostszy gamma-ketonokwas o wzorze półstrukturalnym CH3-CO-CH2-CH2-COOH lub sumarycznym C5H8O3. Sole kwasu lewulinowego to lewuliniany Stosowany jest w syntezie do otrzymywania związków organicznych oraz do produkcji leków.
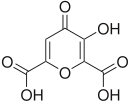
5) Kwas lewulinowy (kwas 4-oksowalerianowy lub kwas gamma-oksowalerianowy) - jest to organiczny związek chemiczny, najprostszy gamma-ketonokwas o wzorze półstrukturalnym CH3-CO-CH2-CH2-COOH lub sumarycznym C5H8O3. Sole kwasu lewulinowego to lewuliniany Stosowany jest w syntezie do otrzymywania związków organicznych oraz do produkcji leków. - 6) Kwas mekonowy - przykład kwasu dikarboksylowego.
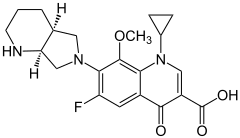 7) Moksyfloksacyna - jest to chemioterapeutyk z grupy flourochinolonów, zaburzający replikację DNA bakterii (inhibitor gyrazy DNA oraz topoizomerazy IV). Działa bakteriobójczo na bakterie Gram-dodatnie (szczepy Staphylococcus aureus wrażliwe na metycylinę, Steptococcus spp. - w tym S. pyogenes i oporne na antybiotyki zczepy S. pneumoniae), bakterie Gram-ujemne (m.in. Haemophilus influenzae, Moraxella catarrhalis, Enrobacter cloacae, Escherichia coli, Klebsiella pneumoniae), bakterie beztlenowe (m.in. Peptosteptococcus spp., Fusobacterium spp.) oraz bakterie atypowe (m.in. Mycoplasma pneumoniae, Legionella pneumophila, Chlamydia pneumoniae). Moksyfloksacyna szybko i niezależnie od pokarmu wchłania się z przewodu pokarmowego (biodostępność około 91%), osiągając stężenie maksymalne we krwi po 0,5-4h. Z białkami osocza wiąże się w 40-42%. Przenika do tkanek układu oddechowego, m.in. do zatok, błony śluzowej oskrzeli i makrofagów pęcherzykowych. Jest metabolizowana w wątrobie.
7) Moksyfloksacyna - jest to chemioterapeutyk z grupy flourochinolonów, zaburzający replikację DNA bakterii (inhibitor gyrazy DNA oraz topoizomerazy IV). Działa bakteriobójczo na bakterie Gram-dodatnie (szczepy Staphylococcus aureus wrażliwe na metycylinę, Steptococcus spp. - w tym S. pyogenes i oporne na antybiotyki zczepy S. pneumoniae), bakterie Gram-ujemne (m.in. Haemophilus influenzae, Moraxella catarrhalis, Enrobacter cloacae, Escherichia coli, Klebsiella pneumoniae), bakterie beztlenowe (m.in. Peptosteptococcus spp., Fusobacterium spp.) oraz bakterie atypowe (m.in. Mycoplasma pneumoniae, Legionella pneumophila, Chlamydia pneumoniae). Moksyfloksacyna szybko i niezależnie od pokarmu wchłania się z przewodu pokarmowego (biodostępność około 91%), osiągając stężenie maksymalne we krwi po 0,5-4h. Z białkami osocza wiąże się w 40-42%. Przenika do tkanek układu oddechowego, m.in. do zatok, błony śluzowej oskrzeli i makrofagów pęcherzykowych. Jest metabolizowana w wątrobie. - MOKSYFLOKSACYNA JEST M.IN. INHIBITOREM GYRAZY DNA.
- *GYRAZA DNA - jest to enzym występujący u Procaryota (szczególnie u bakterii), należący do topoizomeraz typu II. Przy użyciu energii pochodzącej z hydrolizy ATP katalizuje on wprowadzanie ujemnych skrętów w helisie DNA. Enzym składa się z dwóch podjednostek A, które wiążą się kowalencyjnie z rusztowaniem deoksyrybozofosforanowym DNA oraz z podjednostki B, która dostarcza energię rozkładając ATP. Aktywność tych podjednostek hamuje m.in. nowobiocyna. Gyraza odgrywa ważną rolę w procesie replikacji, transkrypcji oraz rekombinacji.
- *CHEMIOTERAPEUTYK to rodzaj substancji chemicznej stosowany w leczeniu chorób zakaźnych. Są to leki przeciwdrobnoustrojowe otrzymane na zasadzie całkowitej syntezy chemicznej, nieposiadające swojego odpowiednika w przyrodzie. Bezpośrednio działanie wszystkich chemioterapeutyków polega na zwalczaniu rozwoju drobnoustrojów w organizmie. Do tej grupy leków należą m.in. sulfonamidy przeciwbakteryjne (w przeciwieństwie do sulfonamidów moczopędnych i przeciwcukrzyczowych).
 9) Ofloksacyna - jest to chemioterapeutyk z grupy fluorochinolonów wykazujący aktywność głównie wobec bakterii Gram-ujemnych, lecz o nieco słabszym działaniu od cyprofloksacyny. Wykazuje natomiast silne działanie w stosunku do bakterii z gatunku Chlamydia, co umożliwia stosowanie jej w zakażeniach miednicy mniejszej przez Chlamydia tachomatis. Nie wykazuje toksycznego działania na wątrobę, co odróżnia ją od większości chinolonów.
9) Ofloksacyna - jest to chemioterapeutyk z grupy fluorochinolonów wykazujący aktywność głównie wobec bakterii Gram-ujemnych, lecz o nieco słabszym działaniu od cyprofloksacyny. Wykazuje natomiast silne działanie w stosunku do bakterii z gatunku Chlamydia, co umożliwia stosowanie jej w zakażeniach miednicy mniejszej przez Chlamydia tachomatis. Nie wykazuje toksycznego działania na wątrobę, co odróżnia ją od większości chinolonów.  10) Kwas pirogronowy (kwas 2-oksopropanowy) - jest to organiczny związek chemiczny z grupy alfa-ketokwasów. Jest produktem przejściowym fermentacji alkoholowej węglowodanów. W organizmach powstaje zwykle jako produkt glikolizy w ciągu reakcji zachodzących w cytozolu. W warunkach tlenowych przekształcenie jednej cząsteczki glukozy do 2 cząsteczek pirogronianu dostarcza 2 cząsteczek ATP i 2 cząsteczek NADH. Pirogronian przekształcony przez kompleks dehydrogenazy
10) Kwas pirogronowy (kwas 2-oksopropanowy) - jest to organiczny związek chemiczny z grupy alfa-ketokwasów. Jest produktem przejściowym fermentacji alkoholowej węglowodanów. W organizmach powstaje zwykle jako produkt glikolizy w ciągu reakcji zachodzących w cytozolu. W warunkach tlenowych przekształcenie jednej cząsteczki glukozy do 2 cząsteczek pirogronianu dostarcza 2 cząsteczek ATP i 2 cząsteczek NADH. Pirogronian przekształcony przez kompleks dehydrogenazy - pirogronianowej do Acetylo-CoA uczestniczy w cyklu kwasu cytrynowego (cyklu Krebsa).

- anion pirogronianowy
- KWASY POLIKARBOKSYLOWE:
 1) Kwas Kempa (kwas cis, cis-1,3,5-trimetylocykloheksano-1,3,5-trikarboksylowy) - jest to organiczny związek chemiczny, kwas trójkarboksylowy będący pochodną cykloheksanu. Związek ten wykorzystuje się do syntezy receptorów molekularnych oraz w badaniach modelowania miejsc aktywnych enzymów. Grupy karboksylowe są w pozycjach aksjalnych, a grupy metylowe w pozycjach ekwatorialnych. Związek ten został otrzymany w 1981 roku przez Daniela S. Kempa. Kwas Kempa jest związkiem, który tworzy z różnymi aminami kryształy o skomplikowanej sieci wiązań wodorowych tworząc struktury supramolekularne.
1) Kwas Kempa (kwas cis, cis-1,3,5-trimetylocykloheksano-1,3,5-trikarboksylowy) - jest to organiczny związek chemiczny, kwas trójkarboksylowy będący pochodną cykloheksanu. Związek ten wykorzystuje się do syntezy receptorów molekularnych oraz w badaniach modelowania miejsc aktywnych enzymów. Grupy karboksylowe są w pozycjach aksjalnych, a grupy metylowe w pozycjach ekwatorialnych. Związek ten został otrzymany w 1981 roku przez Daniela S. Kempa. Kwas Kempa jest związkiem, który tworzy z różnymi aminami kryształy o skomplikowanej sieci wiązań wodorowych tworząc struktury supramolekularne.
Źródło: Wikipedia. Struktura kwasu Kempa obecna w kryształach tego związku.
2) DTPA (kwas pentetynowy, łac. Acidum penteticum) - substancja, której związki chelatowe Ca-DTPA stosowane są do usuwania z organizmu niektórych radionuklidów i metali ciężkich. Jednak głównym zastosowaniem jest dodawanie ich jako składnik pulpy drzewnej przy bieleniu papieru. DTPA ma za zadanie wychwytywać metale, które powodują rozbijanie wody utlenionej. Kompleks DTPA i radionuklidu 99mTc stosowany jest w badaniu diagnostycznym czynności nerek.3) EDTA (kwas wersenowy, kwas edetynowy, komplekson II, łac. Acidum edeticum) - jest to organiczny związek chemiczny, kwas pokikarboksylowy i jednocześnie alfa-aminokwas. Z mocnymi wodorotlenkami tworzy werseniany. Jest on szeroko stosowanym czynnikiem kompleksującym wiele kationów metali (Ca2+, Mg2+, Fe3+, zwykle w postaci soli disodowej - wersenian disodowy ze względu na jej większą rozpuszczalność w wodzie, tzw. komplekson III). Jego skrót pochodzi od nazwy angielskiej: ethylenediaminetetraacetic acid. Ważnym zastosowaniem EDTA jest maskowanie jonów metali - na przykłąd bizmutu, chromu (III), cynku, cyrkonu, glinu, kadmu, kobaltu, magnezu, miedzi, niklu, ołowiu, toru, wanadu, żelaza (III), które jest możliwe w wyniku tworzenia z nimi kompleksów chelatowych. Właściwości chelatujące kwasu wersenowego są na tyle silne, że tworzy on kompleksy nawet z berylowcami.
Kompleks DTPA i radionuklidu 99mTc stosowany jest w badaniu diagnostycznym czynności nerek.3) EDTA (kwas wersenowy, kwas edetynowy, komplekson II, łac. Acidum edeticum) - jest to organiczny związek chemiczny, kwas pokikarboksylowy i jednocześnie alfa-aminokwas. Z mocnymi wodorotlenkami tworzy werseniany. Jest on szeroko stosowanym czynnikiem kompleksującym wiele kationów metali (Ca2+, Mg2+, Fe3+, zwykle w postaci soli disodowej - wersenian disodowy ze względu na jej większą rozpuszczalność w wodzie, tzw. komplekson III). Jego skrót pochodzi od nazwy angielskiej: ethylenediaminetetraacetic acid. Ważnym zastosowaniem EDTA jest maskowanie jonów metali - na przykłąd bizmutu, chromu (III), cynku, cyrkonu, glinu, kadmu, kobaltu, magnezu, miedzi, niklu, ołowiu, toru, wanadu, żelaza (III), które jest możliwe w wyniku tworzenia z nimi kompleksów chelatowych. Właściwości chelatujące kwasu wersenowego są na tyle silne, że tworzy on kompleksy nawet z berylowcami.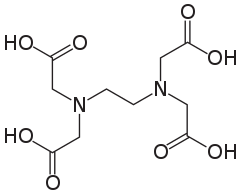 EDTA stosowany jest jako odczynnik kompleksujący w chemii analitycznej; środek konserwujący żywność (wiązanie metali ciężkich - kofaktorów niepożądanych enzymów), składnik roztworów buforowych; zapobieganie pozaustrojowemu krzepnięciu krwi (wiązanie wapnia), stosowany jest ponadto jako odtrutka w zatruciach metalami ciężkimi; stosowany jest w nawozach mikroelementowych; jest inhibitorem metaloproteaz; stanowi składnik uzdatniaczy wody w akwarystyce, jest składnikiem niektórych mydeł; hamuje karbapenemazy (bakteryjne enzymy hydrolizujące wiązanie beta-laktamowe w cząsteczce karbapenemów - rodzaju antybiotyków beta-laktamowych - można je zaliczyć do beta-laktamaz).
EDTA stosowany jest jako odczynnik kompleksujący w chemii analitycznej; środek konserwujący żywność (wiązanie metali ciężkich - kofaktorów niepożądanych enzymów), składnik roztworów buforowych; zapobieganie pozaustrojowemu krzepnięciu krwi (wiązanie wapnia), stosowany jest ponadto jako odtrutka w zatruciach metalami ciężkimi; stosowany jest w nawozach mikroelementowych; jest inhibitorem metaloproteaz; stanowi składnik uzdatniaczy wody w akwarystyce, jest składnikiem niektórych mydeł; hamuje karbapenemazy (bakteryjne enzymy hydrolizujące wiązanie beta-laktamowe w cząsteczce karbapenemów - rodzaju antybiotyków beta-laktamowych - można je zaliczyć do beta-laktamaz). Źródło: Wikipedia. Kompleks chelatowy EDTA z jonem metalu (M).4) EGTA - jest to organiczny związek chemiczny będący związkiem chelatującym. Jest on stosowany w chemii analitycznej. Często jest składnikiem tzw. płynu Krebsa. Właściwości chelatujące podobne do EDTA, w odróżnieniu od niego silniej wiąże jony wapniowe od magnezowych.
Źródło: Wikipedia. Kompleks chelatowy EDTA z jonem metalu (M).4) EGTA - jest to organiczny związek chemiczny będący związkiem chelatującym. Jest on stosowany w chemii analitycznej. Często jest składnikiem tzw. płynu Krebsa. Właściwości chelatujące podobne do EDTA, w odróżnieniu od niego silniej wiąże jony wapniowe od magnezowych. 5) Kwasy fulwowe - są to organiczne związki chemiczne o charakterze kwasowym będące częścią próchnicy glebowej (obok kwasów huminowych i humin). Są one dobrze rozpuszczalne w wodzie, alkoholu, alkaliach oraz w kwasach mineralnych. Kwasy fulwowe (podobnie jak inne substancje humusowe) nie mają ściśle określonego składu i struktury, lecz stanowią umowną grupę cząstek, różniącą się pod względem wielkości, masy cząsteczkowej i właściwości, a wydzielaną na podstawie różnić rozpuszczalności w różnych rozpuszczalnikach. Zbudowane są z pierścieni aromatycznych zawierających liczne grupy funkcyjne (głównie kwasowe grupy fenolowe i karboksylowe) i łańcuchy boczne, powiązane wiązaniami wodorowymi i siłami van der Waalsa. Masa cząsteczkowa jest rzędu kilku tysięcy daltonów. Procentowy udział poszczególnych pierwiastków nie jest stały, jednak różni się wyraźnie od procentowego składu innych związków organicznych. Kwasy fulwowe z procentach atomowych zawierają: 44-49% C, 3,5-7,5% H, 44-49% O, 0,3-4% N. W porównaniu do kwasów huminowych charakteryzują się one prostszą, bardziej jednorodną budową, niższą masą cząsteczkową i większą rozpuszczalnością. Są one od nich teżjaśniejsze, mają mniejszą procentową zawartość atomów węgla, za to więcej struktur alifatycznych.
5) Kwasy fulwowe - są to organiczne związki chemiczne o charakterze kwasowym będące częścią próchnicy glebowej (obok kwasów huminowych i humin). Są one dobrze rozpuszczalne w wodzie, alkoholu, alkaliach oraz w kwasach mineralnych. Kwasy fulwowe (podobnie jak inne substancje humusowe) nie mają ściśle określonego składu i struktury, lecz stanowią umowną grupę cząstek, różniącą się pod względem wielkości, masy cząsteczkowej i właściwości, a wydzielaną na podstawie różnić rozpuszczalności w różnych rozpuszczalnikach. Zbudowane są z pierścieni aromatycznych zawierających liczne grupy funkcyjne (głównie kwasowe grupy fenolowe i karboksylowe) i łańcuchy boczne, powiązane wiązaniami wodorowymi i siłami van der Waalsa. Masa cząsteczkowa jest rzędu kilku tysięcy daltonów. Procentowy udział poszczególnych pierwiastków nie jest stały, jednak różni się wyraźnie od procentowego składu innych związków organicznych. Kwasy fulwowe z procentach atomowych zawierają: 44-49% C, 3,5-7,5% H, 44-49% O, 0,3-4% N. W porównaniu do kwasów huminowych charakteryzują się one prostszą, bardziej jednorodną budową, niższą masą cząsteczkową i większą rozpuszczalnością. Są one od nich teżjaśniejsze, mają mniejszą procentową zawartość atomów węgla, za to więcej struktur alifatycznych. - TYPOWY KWAS FULWOWY.
- TYPOWY KWAS FULWOWY.
- C



Brak komentarzy:
Prześlij komentarz